|
LentiBOOST™:全球 40+ 項臨床試驗首選!實測轉導效能提升 7 倍! 隨著台灣《再生醫療法》與《再生醫療製劑條例》於 2026 年 1 月正式實施,細胞與基因治療 (CGT) 正式邁入法規完備的商業化元年。在臨床開發中,慢病毒 (Lentivirus) 憑藉其能穩定整合至宿主基因組、具備大片段基因載荷能力,以及可感染非分裂細胞等技術優勢,穩居細胞治療載體的首選地位。 然而,如何提升轉導效率 (Transduction Efficiency),始終是研發與製程開發的核心課題。開發者往往需要在追求高轉導成功率、維持細胞活性,以及嚴格控制載體拷貝數 (VCN) 之間取得平衡,以符合嚴謹的法規監管要求。 以 Orchard Therapeutics 於 2024 年獲 FDA 批准的 Lenmeldy 為例,這款治療 MLD 的慢病毒造血幹細胞療法,單劑定價高達 425 萬美元。如此高昂的代價反映了製程開發的難度,也凸顯了如何在維持療效與安全性的同時、有效降低生產成本。對於開發者而言,如何提升病毒載體的使用效率、進而優化生產成本,已成為研發與製程開發中的重要課題。
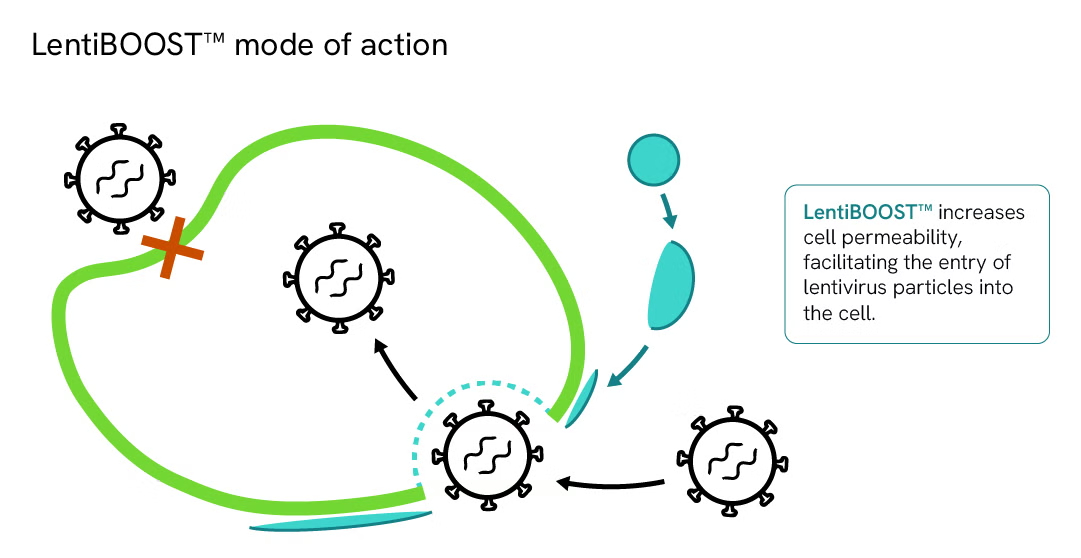
美商 Revvity 旗下的 LentiBOOST™ 技術,即是這一課題的最佳解決方案。這款高效、無細胞毒性、非受體依賴型的 慢病毒(Lentivirus)轉導增強劑,透過促進慢病毒包膜與目標細胞膜的融合,能顯著提升轉導效率。
根據實測數據,LentiBOOST™ 在CD34+ 造血幹細胞 (HSC)、間質幹細胞 (MSC)、初代 T 細胞、NK 細胞及纖維母細胞中,最高可提升轉導效率達 7 倍,不僅能提升治療效能,更能減少慢病毒載體用量,從而大幅降低研發與生產成本。
憑藉優異的特性,這項技術已獲得全球超過 40 項臨床試驗(涵蓋 Phase I 至 III)以及 2 項上市藥物採用。為支援不同階段的開發需求,LentiBOOST™ 提供 Pharma Grade (研發級) 與 GMP Grade (臨床級) 兩種規格,協助開發者實現製程的無縫銜接。 想了解更多 LentiBOOST™ 技術細節? |
||
 |
 |
|
伯森生物科技(股)公司 Blossom Biotechnologies, Inc.
網址 www.blossombio.com 客服 0800-059668
[ 📝 線上留言諮詢
] [ ☎ 伯森業務專員聯絡資訊
]